El grupo de Fisiopatología Cardiovascular del Instituto de Biomedicina de Sevilla, IBiS/Hospital Universitario Virgen del Rocío/US/CSIC, liderado por Tarik Smani y Antonio Ordoñez, consigue financiación para este proyecto en colaboración con el grupo de Fisiología de la Universidad de Extremadura, liderado por Juan Antonio Rosado y Ginés Salido
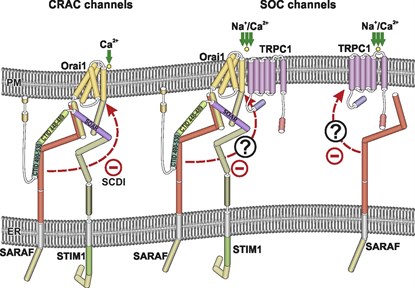
Fig. 1. Descripción general de la regulación de Orai1 y TRPC1 por SARAF. En las células que expresan STIM1, SARAF modula negativamente la entrada de Ca2 + a través de canales CRAC y SOC regulados por STIM1. Además, SARAF atenúa la entrada de cationes a través de la agrupación TRPC1 independiente del flujo de señal STIM1. (Jardín et al., 2018).
El pasado 11 de junio, la Agencia Estatal de Investigación publicó en la sede electrónica del Ministerio de Ciencia e Innovación, la propuesta de resolución provisional de ayudas de la convocatoria 2019 correspondientes a las modalidades de “Proyectos de I+D+i”, en el marco del Programa Estatal de Generación de Conocimiento y Fortalecimiento Científico y Tecnológico del Sistema de I+D+i y del Programa Estatal de I+D+i Orientada a los Retos de la Sociedad, del Plan Estatal de Investigación Científica y Técnica y de Innovación 2017-2020. En dicha convocatoria, resultó financiado el proyecto titulado “REMODELADO: EXPRESIÓN DE STIM Y ORAI Y DE SUS MECANISMOS REGULADORES EN CÁNCER Y ANGIOGÉNESIS”.
La entrada capacitativa de calcio (ECC) es un mecanismo importante para la entrada de calcio regulada por los depósitos intracelulares de calcio y a día de hoy sigue siendo una gran desconocida en diversos procesos celulares. Los elementos clave de la ECC son el sensor de calcio del retículo endoplásmico (ER) STIM1, y su homólogo STIM2, y los canales capacitativos, incluyendo los canales de calcio activados por la liberación de calcio (CRAC), compuestos por Orai1, y el canal activado por los almacenes (SOC), formado por Orai1 y TRPC1. Orai1 tiene dos homólogos, Orai2 y Orai3. Se han identificado dos variantes de Orai1 expresadas de forma ubicua, Orai1alfa, específica de mamíferos, y Orai1beta, que funcionan indistintamente en los canales CRAC y SOC, aunque Orai1alfa muestra una inactivación más pronunciada. También, se han identificado tres variantes de STIM2: STIM2.1, STIM2.2 y STIM2.3. La forma clásica, STIM2.2, activa la ECC en respuesta a pequeños cambios en el calcio reticular. Por contra, STIM2.1 juega un papel inhibidor en la ECC.
Las proteínas STIM y Orai están sujetas a modificaciones postraduccionales, como glicosilación o fosforilación, que regulan su función. El ajuste fino de la ECC también se logra mediante un número creciente de proteínas reguladoras que modulan la interacción STIM1-Orai1, como el regulador de STIM1, SARAF, y el modulador de la asociación STIM1-SARAF, EFHB. La identificación de isoformas y variantes de STIM y Orai funcionalmente diversas, sujetas a modificaciones postraduccionales, y los reguladores de la ECC revelan la complejidad de este mecanismo en un tipo de célula particular.
Desde hace tiempo, el calcio intracelular se ha relacionado con el cáncer. La activación de la ECC se ha implicado en varias características distintivas del cáncer, tales como proliferación, migración, metástasis o resistencia a la apoptosis, así como en la vascularización tumoral y la angiogénesis. Con respecto a la angiogénesis, en las células endoteliales la ECC es muy relevante en los primeros pasos de la angiogénesis, como la proliferación, la migración y la formación in vitro de estructuras capilares; por lo tanto, la caracterización del papel funcional de las isoformas y variantes de STIM y Orai en la señalización de calcio en el contexto de la vascularización tumoral sería beneficiosa para determinar el progreso tumoral. La ECC se remodela de manera diferencial en las células progenitoras endoteliales proveniente de pacientes con cáncer. No obstante, las bases moleculares de la regulación de la ECC en las células endoteliales y sus progenitores no se han caracterizado completamente.
Dada la relevancia de la ECC en el cáncer de mama y la angiogénesis, el objetivo del presente sub-proyecto es caracterizar el remodelado de la ECC en células endoteliales y de músculo liso, y su participación en la angiogénesis. Por ello el gran objetivo de este proyecto es centrarse en las isoformas y variantes de STIM y Orai, su expresión, ubicación subcelular e interacción con proteínas reguladoras y explorar la relevancia funcional de la ECC en la angiogénesis. Los resultados de la presente propuesta podrían ayudar a identificar marcadores de diagnóstico o pronóstico de desarrollo tumoral o potenciales dianas terapéuticas.













